 DOC
DOC
【文档说明】《气体的制取、收集和除杂》导学案-九年级上册化学北京版.doc,共(4)页,553.500 KB,由小喜鸽上传
转载请保留链接:https://www.ichengzhen.cn/view-39582.html
以下为本文档部分文字说明:
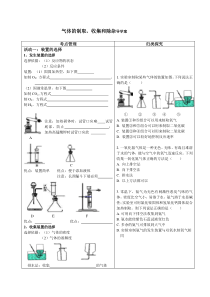
气体的制取、收集和除杂导学案考点管理归类探究活动一:装置的选择1、发生装置的选择选择依据:(1)反应物的状态(2)反应条件装置:(1)固固加热型,如下图如制O2,方程式、(2)固液常温型,如下图如制CO
2,方程式制O2,方程式制H2,方程式注意:加热固体时,试管口应略试管底部,防止;加热高锰酸钾时试管口应放AC优点:装置简单优点:便于添加液体注意:长颈漏斗下端必须DEF优点:优点:2、收集装置的选择选择依据:(1)气体的密度(2)气体的溶
解度排水法:收集的气体1.实验室制取某些气体的装置如图。下列说法正确的是()①②③④⑤A.装置①和⑤组合可以用来制取氧气B.装置②和⑤组合可以用来制取二氧化碳C.装置②和④组合可以用来制取二氧化碳D.装置
②可以较好地控制反应速率2.一氧化氮气体是一种无色、无味、有毒且难溶于水的气体,能与空气中的氧气迅速反应。下列收集一氧化氮气体正确的方法是()A.向上排空法B.向下排空法C.排水法D.以上方法都可以3.常温下,氨气为无色
有刺激性恶臭气味的气体,密度比空气小,易溶于水,氨气溶于水显碱性;实验室可用氯化铵固体和氢氧化钙固体混合加热制取。则下列说法正确的是()A.可用向下排空法收集到氨气B.氨水能使紫色石蕊试液变红色C.多余的氨气可排放到大气中D.实验室制氨气的发生装置与
双氧水制氧气相同向上排空法:收集的气体向下排空法:收集的气体注意:(1)排空法,导管必须伸到集气瓶底部;(2)排水法,当时,才能收集氧气,防止。活动二:气体的净化和干燥1、常见气体的净化原则:所选试剂只能吸收杂质气体,不能吸收待净化的气体,不引入新
的气体杂质除CO2:可用除HCl(CO2中混有的):可通过饱和的NaHCO3溶液除H2:可通过灼热的CuO将其氧化为水净化装置除CO:可通过长进短出2、气体干燥常见干燥剂浓硫酸NaOH固体生石灰干燥装置不可干燥的气体不可干燥等碱性气体
不可干燥等酸性气体提示:先除杂,后干燥4.除去下列物质中所含少量杂质的方法,其中不正确的是()A.CO2中混有CO:通过灼热的氧化铜B.H2中混有水蒸气:通过盛有浓硫酸的洗气瓶C.CO中混有CO2:通过氢氧化钠溶液D.CO2中有气体HCl:通过氢氧化钠溶液5.下列各组气体中,均能用固
体氢氧化钠干燥的一组是()A.H2、O2、HClB.H2、O2、COC.H2、CO、SO2D.O2、CO、CO2活动三:尾气处理原则:有毒或污染环境的气体必须进行尾气处理1.CO可用、等方法处理2.H2S、SO2、NH3、Cl2可用液体吸收(装置如下)或用气球收集等方法处理,其中下图中倒置漏斗
的作用:6.SO2通常是一种无色有刺激性气味的有毒气体,密度比空气大,易溶于水,排放到空气中会形成酸雨.实验室用如图装置收集一瓶干燥的S02,装置中的X是.装置的导管按气流方向连接的顺序是→→→→e(填字母),综合训练1.下图是实验室常用的装置
。请据图回答:⑴收集某气体只能采用E装置,由此推测该气体具有的性质⑵用高锰酸钾制取氧气的装置组合是(填序号),反应的化学方程式;若将装置B和C连接进行此实验,实验结束,停止加热前要先将导管移出水面,目的是。⑶实验室制得的CO2气体中常含有HCl和水蒸气。为了
得到纯净、干燥的CO2气体,除杂装置的导管气流方向连接顺序是(填选项)。A.a→b→c→dB.b→a→c→dC.c→d→a→bD.d→c→b→a课后作业:1.在实验课上,同学们设计了实验室制氢气并测定生成氢气体积的实验(装置如图).请回答
下列问题:⑴实验过程中观察到装置B中的现是.⑵C装置的作用.2.如图所示装置,排空法收集二氧化碳时,二氧化碳从进;收集氢气时,氢气从进;装满水收集氧气,氧气从进。3.下图为实验室制取某些气体的装置示意图,据此回答有
关问题(1)写出图中序号①的仪器名称_________________。(2)实验室用双氧水和二氧化锰制取氧气,反应的化学方程式为_____________;其中二氧化锰的作用是___________________________;若选用E装置收集氧气,气体应从___
___端(填a或b)进入,如何检验氧气已满。(3)检查A装置气密性的方法为______________________________。(4)通常状况下,甲烷是一种无色无味气体、难溶于水、密度比空气小。实验室常用醋酸钠和碱石灰两种固体混合加
热制得,制取并收集甲烷可选用的装置是_________。(填字母)4.航天科技飞速发展,密闭的飞船舱中是如何获得氧气并净化舱里的空气呢?为探究其反应原理,某化学兴趣小组的同学,在老师的指导下.进行了如下实验探究.【查阅资料】常温下,过氧化钠(Na2O2
)固体与水反应,生成氢氧化钠和氢气,过氧化钠固体与二氧化碳反应生成碳酸钠和氧气.【实验目的】探究二氧化碳与过氧化钠反应成氧气,并收集干燥纯净的氧气【实验步骤】该小组同学根据实验目的,作出了如下实验设计,请你参与并回答下列问题:(1)写出标号仪器的名称:ab.(2)
实验室常用装置B来制取二氧化碳,反应的化学方程式为:,现要得到纯净干燥的CO2与Na2O2反应,选择装置的组合顺序是B→→E→F(填装置编号),你选择该装置的目的是:(3)若要收集到纯净干燥的氧气,还需将上述
所得氧气先通装置C、E,最后用装置G来收集,其中装置C中反应的化学方程式为.装置E的作用是:【反思与评价】(4)反应后装置F中的过氧化钠固体是否完全反应?取少量该固体与试管中,加入水后观察到有产生,说明过氧化钠没有完全反应.(5)某同学还想到实验室用装置A也
能制得氧气,反应的化学方程式为:,但小组同学讨论后一致认为,飞船舱内不能用此法提供氧气请说明理由:(合理即可)aABCDEFGNaHCO3溶液浓硫酸Na2O2cdabNaOH溶液
 辽公网安备 21102102000191号
辽公网安备 21102102000191号
 营业执照
营业执照