 PPT
PPT
【文档说明】《原子结构示意图、相对原子质量》PPT课件2-九年级上册化学沪教版.ppt,共(13)页,435.500 KB,由小喜鸽上传
转载请保留链接:https://www.ichengzhen.cn/view-36843.html
以下为本文档部分文字说明:
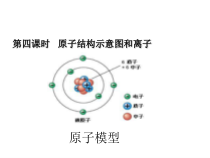
原子模型第四课时原子结构示意图和离子核外电子排布•电子在核外是怎么作高速运动的?电子多了会不会出现“撞车”现象?会不会被原子核吸掉?会不会飞到原子的外面来?•原子核的半径约为原子半径的十万分之一,电子在核外作高速运动。核外电子是分层排布的•第一电子层离核最近、能
量最低,最多能容纳2个电子。•第一层排满后,电子排在第二层,第二层上最多可容纳8个电子。•第三层上最多可容纳18个电子•……•最外层上最多可容纳8个电子(第一层作为最外层时,最多2个)。+16第1层第2层第3层原子核带正电质
子数286原子核电子层原子结构示意图说明电子数稳定结构•最外层电子数为8的结构是稳定结构(He为2个)。•最外层电子数为1-4个的一般为金属原子,最外层电子数为多于4个的一般是非金属原子,最外层电子数为8个的是稀有气体(H
e为2个)。•化学性质活泼或稳定主要取决于原子的最外层电子数。金属原子容易失电子,非金属原子容易得电子,稀有气体性质稳定(一般不参与化学反应)。一、原子的构成1、原子原子核(+)核外电子()质子(+)中子(不带电)(电中性)2、原子中:核电荷数=质子数=核外电子数相对原
子质量=质子数+中子数原子结构示意图氢氦锂铍硼碳氮氧氟氖HHeLiBeBCNOFNe钠镁铝硅磷硫氯氩钾钙NaMgAlSiPSClArKCa1234567891011121314151617181920原子结构示意图说明元素最外层电子数原子结构变化趋势化学性质稀有气体元素金属元素非金属元素决定了
元素的化学性质各元素原子最外电子数目的特点:易失电子稳定易得电子8(He为2个)一般﹤4一般≥4,﹤8相对稳定结构不稳定结构不稳定结构稳定活泼活泼原子最外层电子数【练习】1、下列数据中属于原子质量的属于原子的相对原子质量的A.18gB.21C.1.6×10-26D.3.2×10
-26kg2、计算下列物质的相对分子质量(1)氯气(Cl2)(2)高锰酸钾(KMnO4)(3)硫酸铵[(NH4)2SO4](4)碱式碳酸铜[Cu2(OH)2CO3]3.下列物质由原子直接构成的是()A.水B.二氧化碳C.金刚石D.氧气4.
分子和原子的主要区别是()A.分子一定比原子大B.是否能直接构成物质C.在化学变化中本身是否发生了变化D.是否在不断地运动钠与氯气的反应218+11钠原子(Na)278+17氯原子(Cl)失去1个电子+1128钠离子(Na+)
阳离子得到1个电子288+17氯离子(Cl-)阴离子Na+Cl-
 辽公网安备 21102102000191号
辽公网安备 21102102000191号
 营业执照
营业执照