 DOC
DOC
【文档说明】《溶液的专题复习》教案-九年级下册化学北京版.docx,共(3)页,55.473 KB,由小喜鸽上传
转载请保留链接:https://www.ichengzhen.cn/view-39807.html
以下为本文档部分文字说明:
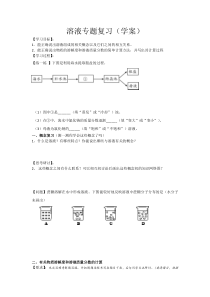
溶液专题复习(学案)【学习目标】:1.能正确说出溶液组成的相关概念以及它们之间的相互关系。2.能正确说出物质的溶解度和溶液质量分数的简单计算方法,并写出其计算过程【学习过程】:【练一练】下图是利用海水提取粗盐的过程。(1)图中①是_____
__(填“蒸发”或“冷却”)池。(2)在①中,海水中氯化钠的质量分数逐渐______(填“变大”或“变小”)。(3)母液为氯化钠的______(填“饱和”或“不饱和”)溶液。一、概念复习(测一测你学会这些概念了吗)1、什么是溶液?有哪些特点?你能说出哪些与溶液有关的概念?【思考研讨】:
2、这些概念之间有什么联系?可以相互间讨论后画出这些概念间的知识网络图?【问题】蔗糖溶解在水中形成溶液。下图能较好地反映溶液中蔗糖分子分布的是(水分子未画出)二、有关物质溶解度和溶液质量分数的计算【要求】:先定思确考
解题思路、并把解题过程书写在题目下面,后与同学交流研讨。(看清题目,依据你对概念的理解,相信自己会很快写出正确答案的)【例】:在t℃时将25g某纯净物加入到100g水中,求所得溶液的溶质的质量分数度。【练习
】如图为X、Y、Z三种固体物质的溶解度曲线,请回答下列问题:1、观察图示判断t30CX、Y、Z的溶解度由小到大的顺序为_____________图中两个交点表示的意义分别是_________________;2、t2℃使Z从其不饱和溶液中析出采取的方法是______。t1℃时使X的饱和溶
液能继续溶解固体X的方法是______;3、t2℃时,Y物质的饱和溶液中,溶质、溶剂、溶液的质量之比为_____,其质量分数是___.4、分别将X、Y、Z的饱和溶液从t30C降温到t10C时,三种溶液中溶质的质量分数由
大到小的顺序是_____.【解题过程用到的重要知识点及得到的启示】:三、课堂小结(通过前段的学习,把你用到的关于溶解度及溶液质量分数的相关计算公式及计算方法和技巧总结出来,找出你认为最好的与同学分享。)【检测与作业】:1、请
从24-A或24-B两题中任选1个作答,若两题均作答,按24-A计分。24-A24-B已知某温度下NaCl的溶解度为25g。现要配制该温度下的NaCl溶液200kg,需要NaCl和水的质量分别是,。配制该溶液的步骤为。今有100kg溶质质量分数为10%的NaOH
溶液稀释为8%的营养液,则需要加水的质量为,称量NaOH固体时用到的仪器为。
 辽公网安备 21102102000191号
辽公网安备 21102102000191号
 营业执照
营业执照